| Unterschied relative und absolute Chronologien in der Archäologie bzw. auch in der Geologie:
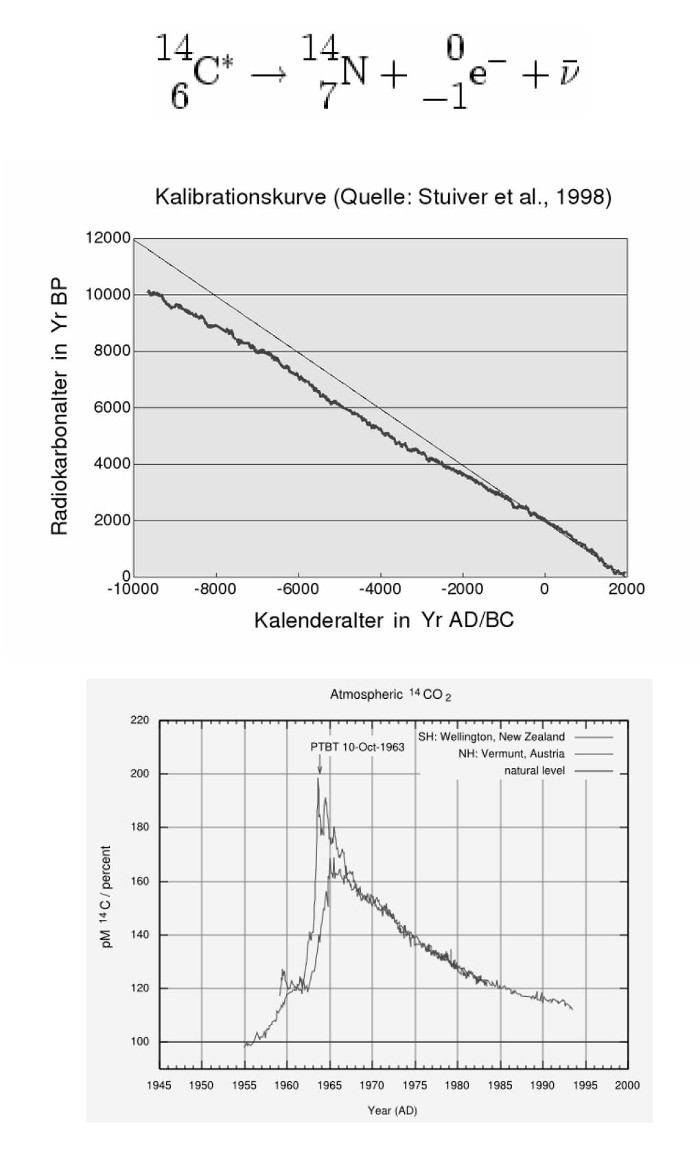
RELATIV: Stratigraphien: Älter/jünger – arch. Objekte terminus post quem; ähnlich mit Leitfossilien in der Geologie; Sedimentablagerungen (Warven) Geologie: Bestimmte zeitlich begrenzte Meteoriteneinschläge lassen sich um die ganze Erde herum nachweisen. Eisbohrkerne Magnetostratigraphie → nur absolut wenn in Raster einhängbar ABSOLUT: Baumringe – Dendrochronologie Thermolumineszenzmethode: Radiaktive Substanzen setzen in Keramik bzw. Rohstoffen Energie frei, die dann in sog. metastabilen Elektronenzuständen gespeichert wird. Je älter desto mehr Energie enthalten. Durch Brennen „innere Uhr“ auf 0 gesetzt. Beim Erhitzen wird diese Energie in Form von Licht wieder frei, dieses kann gemessen werden – Methode ist aber sehr kompliziert da viele Variable (äußere Einflüsse müssen individuell berücksichtigt werden) – geht bis mindestens 50.000 Jahre (mehr als C13, manchmal bis zu 500.000) aber +/- 10% (Datierung Hüttenlehm sinnvoll, aber nur begrenzt brauchbar). Aber vor allem Arbeit mit Konzentrationen versch. radioaktiver Isotope. Genauigkeit und Reichweite derselben je nach Halbwertszeit des Isotops. In der Geologie große Halbwertszeit versch. Isotope (Halbwertszeit>1Mrd.J): Am wichtigsten Uran 238 oder 235→ Blei (Uran-Blei-Datierung) und Kalium 40 → Argon; (Kalium-Argon-Datierung) Uran-Blei-Datierung älteste Proben Sonnensystem (aus Meteoriteneinschlüssen) 4.567 Mio. Jahre; älteste Gesteine auf der Erde (Australien) 4.404 Mio. Jahre. Für die Archäologie natürlich unbrauchbar, dort C14-Methode Entwickelt 1949 von Frank Libby (US-Chemiker), dafür 1960 Nobelpreis für Chemie. Grundlagen: Kohlenstoff kommt in der Natur in den Formen C12, C13 und C14 vor. C12 (98,89%) und C13 (1,11%) sind stabil, aber C14 nicht – sog. Radiokohlenstoff. Zerfällt, wird aber auch durch die Natur ständig nachgebildet. Im ersten Arbeitsschritt einer C14 Datierung geht man davon aus, dass die C14 Konzentration konstant bleibt. Es entsteht in den oberen Schichten der Atmosphäre ständig durch die Kollision von kosmischer Strahlung mit Atomen. Dabei wird ein Neutron freigesetzt, das dann durch eine Kernreaktion ein Proton aus einem Stickstoffatom drängt. Beim Zerfall des C14-Atoms spaltet sich das Neutron wieder in ein Elektron und ein Proton und es entsteht wieder ein N14 Stickstoffkern. C14 ist daher ein Beta-Strahler (Elektronenstrahlung, 5730a). Das in der Atmosphäre gebildete C14 verbindet sich mit Luftsauerstoff zu Kohlendioxid und gelangt dann weiter in den Photosynthesekreislauf und daher praktisch in alle lebenden Organismen. Da diese während ihres Lebens ständig Kohlenstoff mit der Umgebung austauschen bleibt die Konzentration Zeit ihres Lebens konstant, ab ihrem Todeszeitpunkt findet kein Austausch mehr statt und das innere Uhrwerk beginnt zu schlagen (TODESZEITPUNKT). Je älter eine Substanz desto weniger C14 ist in ihr enthalten – wenn man die Konzentration desselben feststellt, kann man also das Alter der Probe bestimmen. Der Anteil von C14 an Kohlenstoff ist etwa ein ppt (1 Teil pro Billion), die Nachweisgrenze liegt bei etwa ein ppq (1 Teil pro Billiarde). Das ist nach etwa 10 Halbwertszeiten erreicht, daraus ergibt sich Reichwerte von max. etwa 50.000 Jahren (In Österreich Großteil des archäologischen Spektrums damit abgedeckt, bis zu 300.000 Jahre nur vereinzelt, andere Datierungsmethoden). Untersuchung: 1. Gewinnung des reinen Kohlenstoffs (in der Form von CO2) aus der Probe. Mit verschiedenen Säuren und Metallen alle anderen Elemente herausgelöst/reduziert. Libby-Zählrohr: Klassische Methode, CO2 als Gas in Zählrohr. Problem: Moderner Kohlenstoff: 3 Zerfälle pro Sekunde pro Moll, alter natürlich noch viel weniger. Aber mehr als 40.000 Messungen notwendig. Große Mengen Probenmaterial (bis 1kg Ausgangsmaterial) und geringe Präzision. Flüssigszintillationsspektrometrie Am Häufigsten: CO2 in Benzol umgewandelt, mit spezieller Substanz die Zerfallenergie in Lichtblitze umwandelt. Präziser als Libby-Zählrohr Beschleuniger-Massenspektrometrie Am modernsten, arbeitet mit Graphit. Viel geringere Mengen notwendig, direkter Nachweis (nicht über Zerfall). Aber viel aufwändiger und teurer. Damit kann man mit der Formel für den radiaktiven Zerfall das unkalibrierte Alter angeben, das konventionelle C14-Alter (in Jahren vor 1950 BP before present). Dieses stimmt aber nicht (jünger als tatsächliches), da c14-Konzentration erdgeschichtlich nicht konstant, wenn auch über die Erde immer gleichmäßig verteilt. Periodische Schwankungen hängen zusammen vor allem mit Sonnenflecken aber auch Änderungen des Erdmagnetfelds. Zu manchen Zeitpunkten Proben aus mehrere 100 Jahren gleiche C14-Konzentration (Bandkeramik, Endneolithikum). Aus Dendrokurven Referenzwerte bekannt (Kalibrationskurven – 24k ad; wenn Probenabfolgen bekannt für Feindatierung verwendbar!), mit denen man gegenrechnen kann. Calibriertes C14 Alter dann meist BC/AD. Fehlerquellen: Nachträglicher C-Eintrag (von jüngerem oder älterem Material) zB. in Höhlen CO2 (Carbonat), Fische in Antarktis mehrere 100 C14-a alt. Nachträgliche Kontamination (Ausgrabungen Alufolie [Lichtempfindlich]) Zusätzlich modern C14-Haushalt völlig durcheinandergeworfen, erstens durch Industrialisierung und zweitens durch Kernwaffentests, die große Mengen an C14 erzeugt haben (siehe Grafik) |
Download: Altersbestimmung mit rad. Isotopen Abbildungen.pdf (3688 Downloads )
